Software di gestione EU MDRdi qualitàdi progettazionedi basi di dati
Aggiungi ai preferiti
Confronta con altri prodotti
Vuoi acquistare direttamente?
Vai sul nostro Shop.
Caratteristiche
- Funzione
- di gestione, di qualità, di progettazione, di basi di dati, di sicurezza, di monitoraggio, della catena di fornitura, di etichettatura
- Applicazioni
- di processo, medicale
- Tipo
- centralizzato
- Altre caratteristiche
- su misura
Descrizione
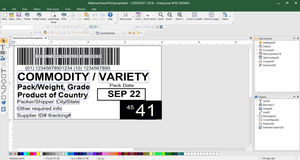
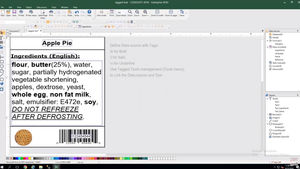
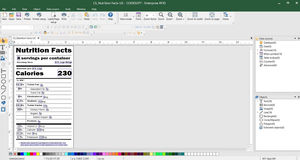
Crea e stampa facilmente etichette conformi EU MDR
CODESOFT per la creazione di etichette EU MDR
Creazione di codici a barre Health Industry Barcode (HIBC) e GS1 Databar
Procedure guidate intuitive
Crea diritti degli utenti e consenti i controlli di sicurezza delle etichette
TEKLYNX CENTRAL CFR per la gestione delle etichette
Estrai gli elementi dell’etichetta da un database centralizzato per etichette conformi EU MDR
Automatizza il processo di etichettatura con la gestione centrale per garantire l’applicazione del processo e un controllo supplementare
Le organizzazioni che distribuiscono dispositivi medici in tutta l'UE devono conformarsi al regolamento EU MDR stabilito nel maggio 2017.
Il Regolamento UE sui Dispositivi Medici (MDR) è progettato per garantire la salute pubblica e la sicurezza dei pazienti in tutta Europa e per aumentare la qualità e la trasparenza dei dispositivi medici nella supply chain sanitaria attraverso la standardizzazione della progettazione delle etichette, dell'approvazione delle etichette e del tracciamento delle etichette.
Di conseguenza, tutte le etichette dei dispositivi medici, ad eccezione dei dispositivi su misura e dei dispositivi per studi di performance/investigativi, dovranno riportare un Identificatore Unico di Dispositivo (UDI), che comprende un Identificatore di Dispositivo (DI), un Identificatore di Prodotto (PI) e un'Informazione Leggibile dall'Uomo (HRI). I produttori e i distributori di dispositivi medici in Europa devono aderire agli standard di etichettatura MDR dell'UE.
Cataloghi
Nessun catalogo è disponibile per questo prodotto.
Vedi tutti i cataloghi di TEKLYNXRicerche correlate
- Soluzione software di automatizzazione
- Soluzione software di gestione
- Soluzione software di analisi
- Soluzione software di processo
- Soluzione software Windows
- Software CAD
- Soluzione software di regolazione
- Soluzione software in tempo reale
- Software in linea
- Soluzione software di progettazione
- Software di interfaccia
- Software di qualità
- Software automatizzato
- Soluzione software di rete
- Soluzione software di sviluppo
- Soluzione software per reportistica
- Software per test
- Software di creazione
- Software 2D
- Software di sicurezza
* I prezzi non includono tasse, spese di consegna, dazi doganali, né eventuali costi d'installazione o di attivazione. I prezzi vengono proposti a titolo indicativo e possono subire modifiche in base al Paese, al prezzo stesso delle materie prime e al tasso di cambio.